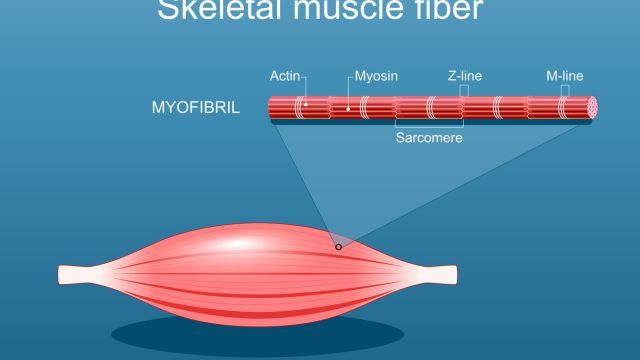
Скелетные мышцы состоят из тысяч волокон двух основных типов: медленные поддерживают осанку и выносливость при длительных нагрузках, а быстрые обеспечивают силу при прыжках или спринте.
Каждое волокно имеет определенный белковый состав, который точно определяет, как оно укорачивается.
Исследование команды из Университета Висконсин-Мэдисон, опубликованное в журнале Журнал масс-спектрометрииописывает технику анализа каждого мышечного волокна в отдельности. С помощью метода в саркомере (структуре внутри волокна, которая укорачивается при сокращении и таким образом приводит в движение мышцу) было обнаружено 37 форм белков. Каждый из них напрямую связан с тем, насколько быстро и сильно укорачивается волокно.
Почему отдельные мышечные волокна отличаются друг от друга?
Скелетные мышцы состоят из двух основных типов волокон. Медленно сокращающиеся волокна типа I поддерживают осанку и выносливость во время длительных тренировок, а быстросокращающиеся волокна типа IIA и IIX обеспечивают взрывную силу при прыжках или спринте. Соотношение между двумя типами мышечных волокон индивидуально и определяет двигательные возможности каждого организма.
Протеомика мышц (изучение белкового состава мышечных волокон) до сих пор изучала мышечную ткань в целом, не выделяя внутри нее отдельные волокна. В большинстве методов анализа белков белки перед измерением разбиваются на пептиды (короткие цепочки аминокислот, из которых состоят белки), чтобы облегчить их распознавание. Эта процедура определяет, какие белки присутствуют в ткани, но теряет информацию о протеоформах (конкретных версиях белка, возникающих в результате генетических особенностей или химических изменений после его синтеза). Именно эти версии определяют, как именно укорачивается каждое волокно.
Что показывает анализ каждого мышечного волокна в отдельности?
Исследование проводилось на волокнах из латеральная широкая мышца (большая мышца бедра), из клеток которой с помощью химических веществ была удалена клеточная мембрана, чтобы добраться до саркомера (структуры внутри волокна, которая укорачивается при сокращении и таким образом приводит в движение мышцу). Каждое волокно прикрепляется к специальному устройству, которое фиксирует силу и скорость, с которой оно укорачивается при стимуляции, и только после этого подвергается анализу белка. Это позволяет напрямую сравнивать данные о сокращении и данные о составе белка каждого волокна, а не получать их косвенно из усредненных измерений всей мышцы.
В новом методе исследуется одно волокно, вес которого измеряется в микрограммах. Клетчатка растворяется в химическом растворе при комнатной температуре, при этом клеточная структура разрушается, а белки высвобождаются в целости и сохранности. Затем белки разделяют по их физико-химическим свойствам и идентифицируют по массе. Это позволяет определить не только какой белок присутствует в клетчатке, но и в какой именно версии он находится и претерпел ли он химические изменения с момента своего синтеза.
В результате анализа в саркомере обнаружено 37 форм белков, в том числе:
- Тропонины – которые запускают сокращение в тот момент, когда уровень кальция в клетке повышается;
- Легкие цепи миозина – от них зависит, с какой силой и скоростью укорачивается волокно.
Состав белка варьируется не только между участниками исследования, но и между волокнами одной и той же мышцы одного и того же участника. Также было обнаружено, что альфа-тропомиозин (палочковидный белок, который регулирует, когда нити актина и миозина вступают в контакт и вызывают сокращение мышц) фосфорилируется в некоторых волокнах, но не в других — изменение, которое напрямую влияет на его активность.
Что эта изменчивость означает для здоровья мышц?
Исследование проводилось на шести участниках, что является стандартным ограничением при разработке нового метода. Оборудование требует высокого разрешения, а работа с таким небольшим количеством материала требует специальных знаний, что на данный момент ограничивает его широкое применение. В более крупной выборке метод может оказаться полезным при изучении саркопении (постепенная потеря мышечной массы и силы с возрастом) и миопатий (заболеваний, при которых мышечная ткань повреждается или теряет свою функцию).
Подробнее о мышцах можно прочитать в В чем секрет роста мышц? | Пульс.бг
Ссылки:
1. Уилсон М.К., Гао З., Лопес Дж.Р. и др. Нисходящая протеомика мышечных волокон человека с кожей выявляет изменчивость между волокнами с разрешением протеоформ. J Масс-спектр. 2026;61(3):e70040. doi:10.1002/jms.70040.
2. Мелби Дж.А., Браун К.А., Грегорич З.Р. и др. Высокочувствительная протеомика сверху вниз фиксирует гетерогенность отдельных мышечных клеток в крупных протеоформах. Proc Natl Acad Sci US A. 2023;120(19):e2222081120. doi:10.1073/pnas.2222081120.
3. Мургия М., Чисилиот С., Нагарадж Н. и др. Признаки неиспользования мышц во время космического полета и постельного режима, выявленные с помощью протеомики отдельных мышечных волокон. ПНАС Нексус. 2022;1(3):pgac086. doi:10.1093/pnasnexus/pgac086.